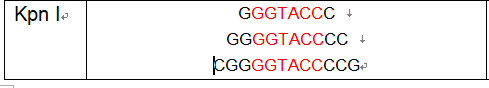导读:
在分子生物学研究中,引物的设计是非常重要的一步,因为它直接影响到PCR扩增的特异性和灵敏度。以下是以猪的G6PD基因为例,介绍一下引物设计的步骤。
1.首先我们得到G6PD的CDS序列
1.1 打开NCBI,在下拉框里面选择Gene数据库(图1.1),然后输入G6PD进行搜索。
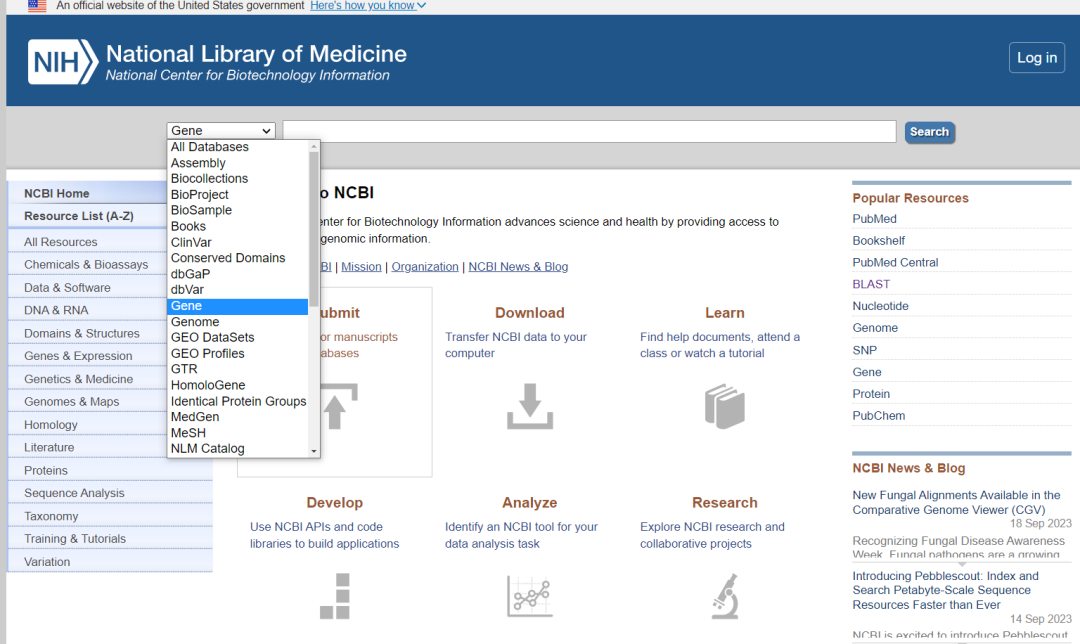
1.2 选择对应物种的G6PD基因,我们这里选择克隆猪的G6PD基因(SUS),可以根据需要,选择其他物种。
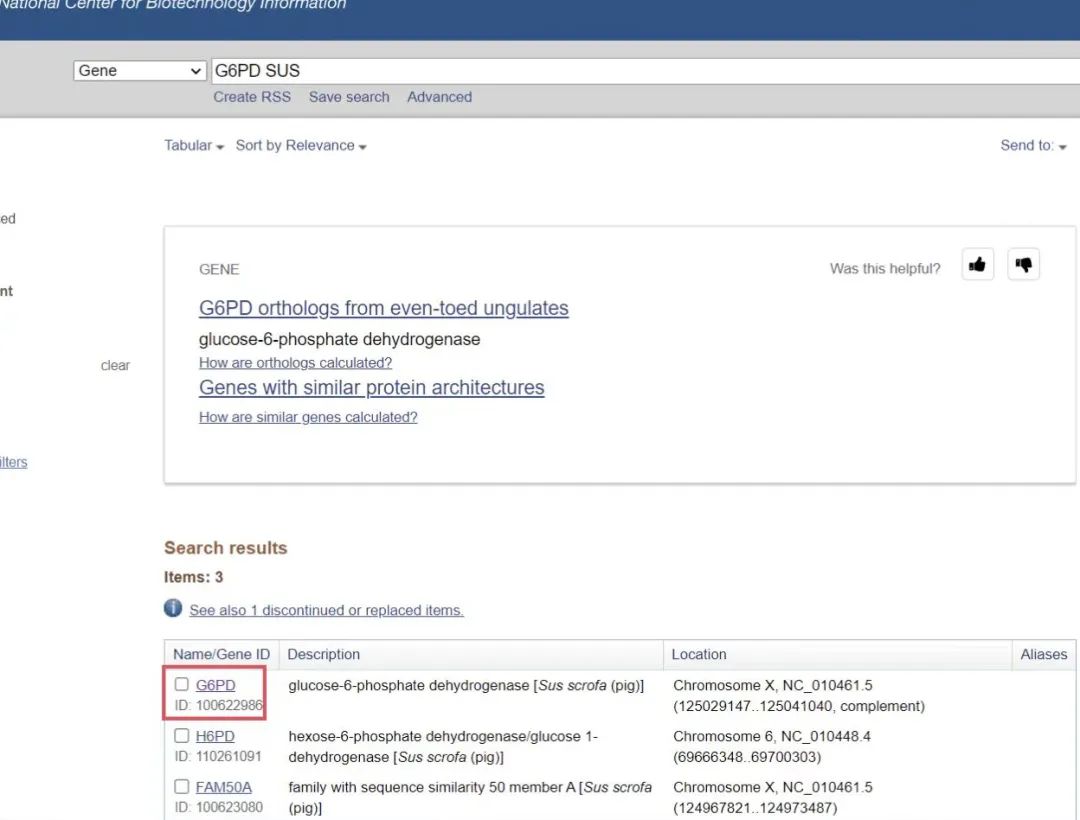
1.3 在G6PD基因的页面中,有非常多的信息,我们往下找到mRNA and Proteins栏目。
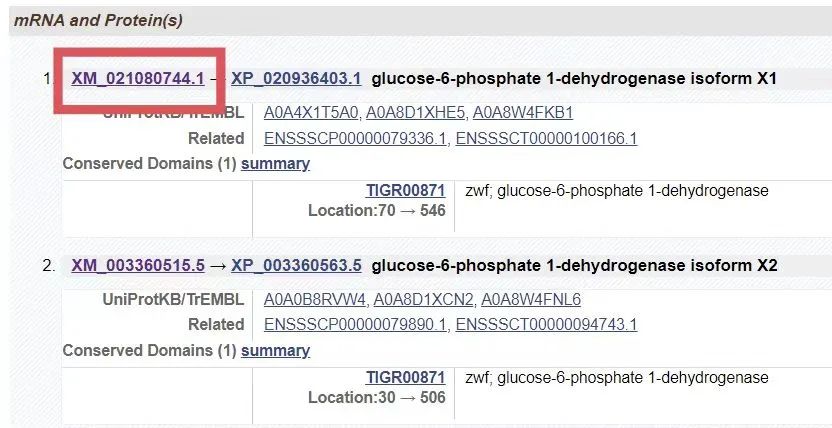
1.4 在新的网页中,我们找到如下图的CDS链接并点击。
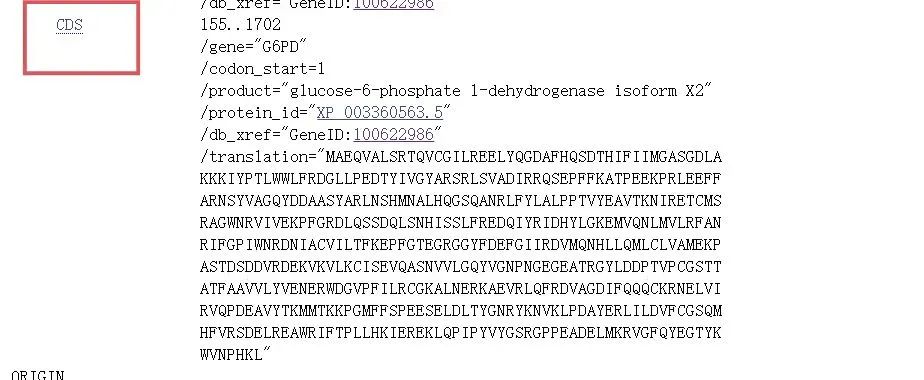
1.5 点击CDS链接之后如下图所示。
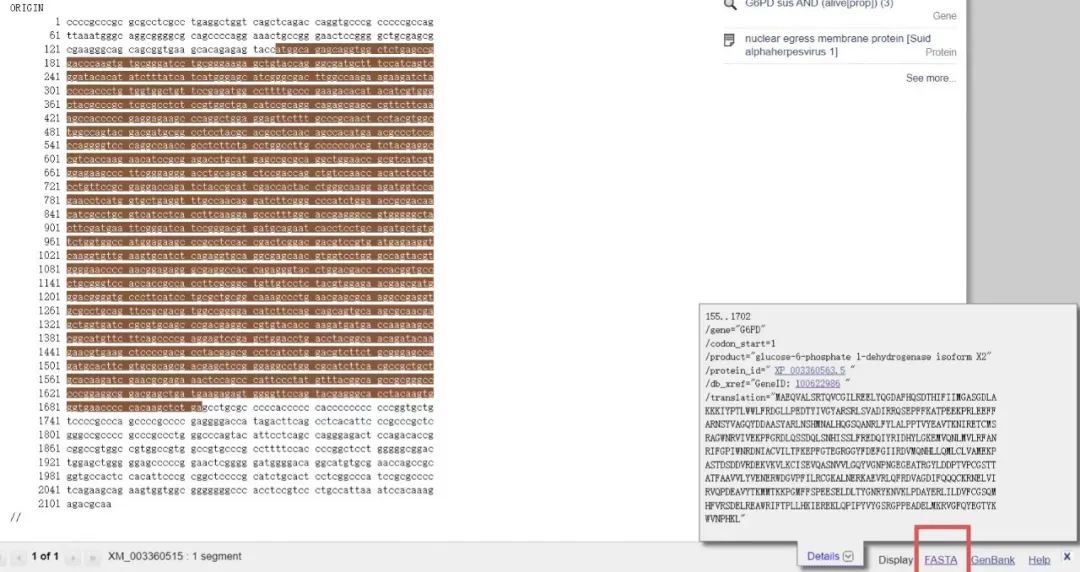
1.6 接下来点击上图中的红色框“FASTA”,得到如下结果,从ATG开始到TGA结尾为G6PD的CDS区。我们把这段序列粘贴到一个记事本中,用于后面操作。

2.获得G6PD的上下游引物
2.1 打开软件Gene Tool
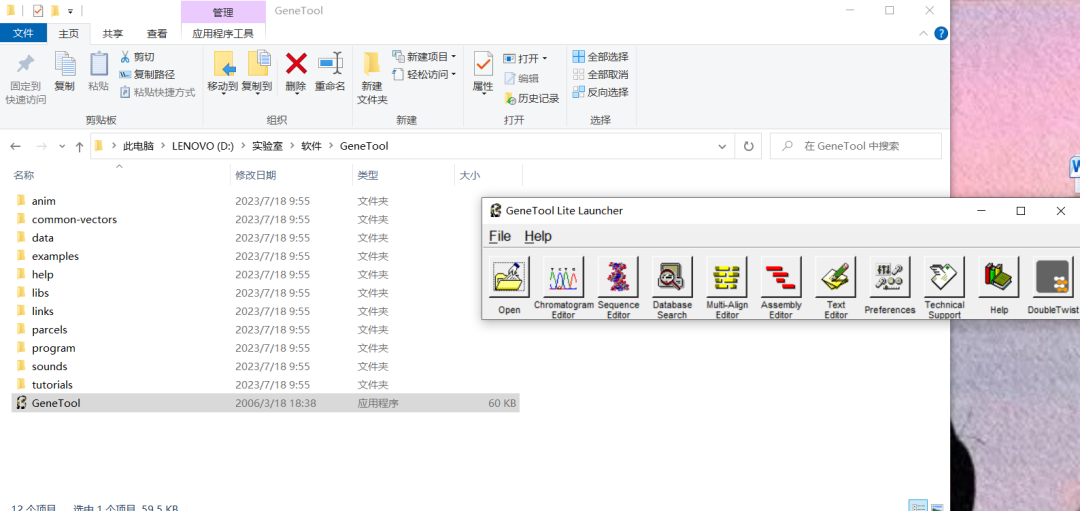
2.2 点开File,打开New Sequence Editor,将G6PD mRNA序列复制,点击Analyze的Find PCR Primers。
2.3 得到以下结果
2.4 通过从目的基因的5'端和3'分别设计引物,设计得分比较高,退火温度接近的引物序列。
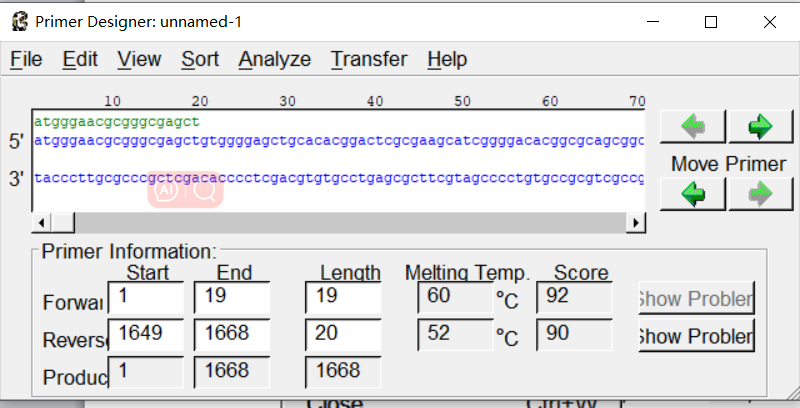
2.5 将设计的引物导出,点击File save Primer As ,得出上下游引物序列。

2.6 判断获取的引物特异性。我们在NCBI数据库中检测这对引物的特异性。打开:http://blast.ncbi.nlm.nih.gov/Blast.cgi 选择标识的Primer Blast

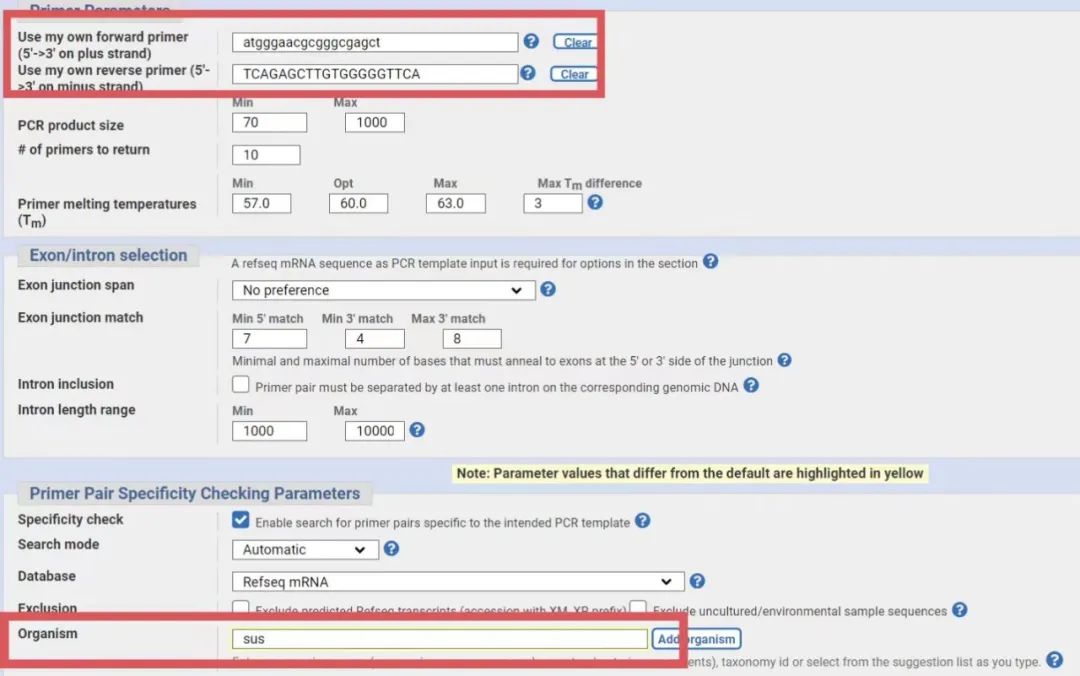
2.7 在出来的网页中,把中得到的引物分别输入,选择种属。其他参数不要修改,然后 点击最下面的Get Primer.
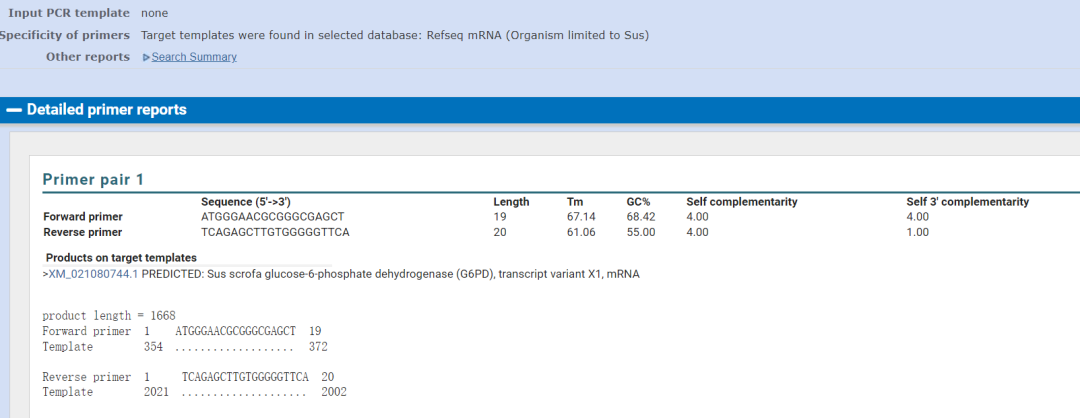
2.8 经过一段时间等待后,出来了如下页面,该页面中100%匹配的只有G6PD,证明引物特异性可以。如果引物的退火温度以及特异性不够,可以增加引物的长度。
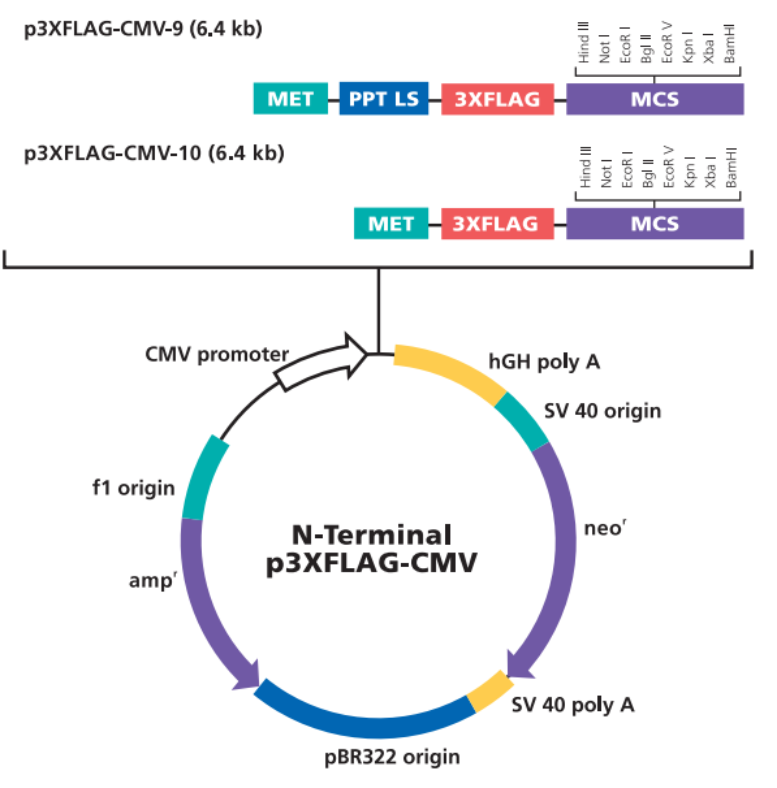
3.选择合适的表达载体
我们选择表达载体。比较常用的了3×FLAG-CMV-10/14, pEGFP-N1 pEGFP-C1等,我们在这选择3×FLAG-CMV-10。
3.1 T4连接
选择双酶切的两个酶要满足如下条件:
(1) 两个酶在载体中存在。
(2) 两个酶不存在于目的蛋白的CDS中。
(3) 两个酶应该具有共同酶切的Buffer。
3.1.1 确定目的基因上有哪些酶切位点,可以用以下软件
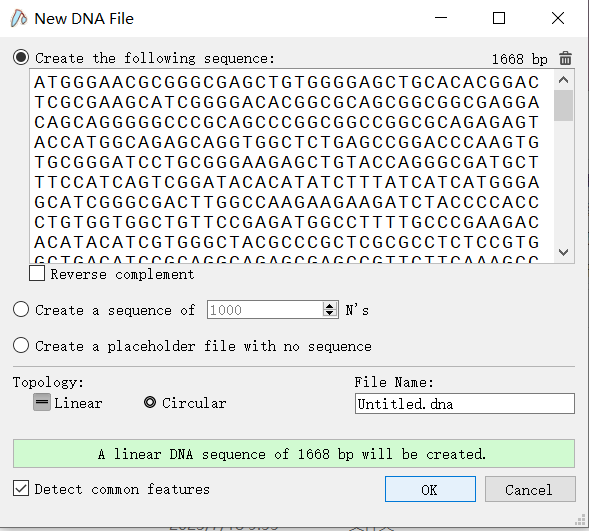
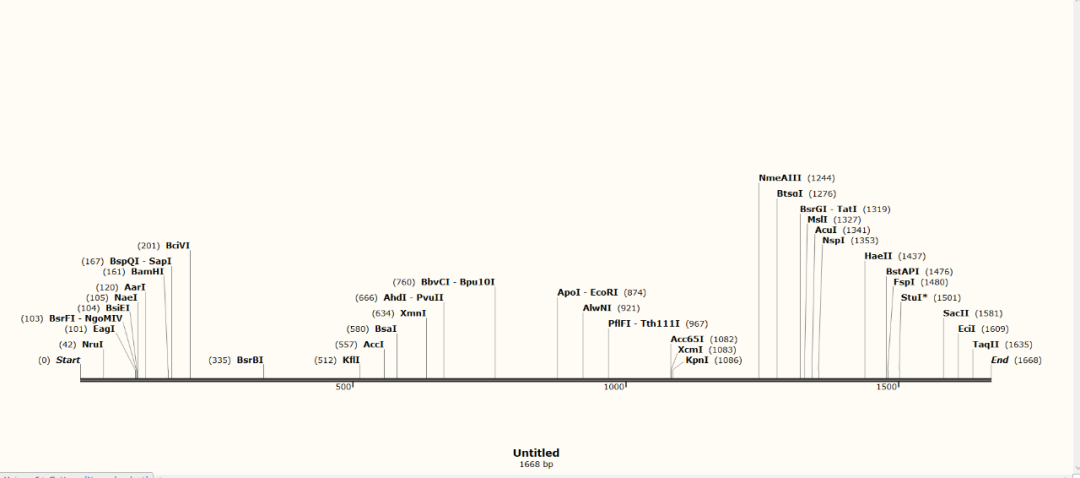
3.1.2 通过筛选发现除BamHI、EcoRI、KpnI都可以用
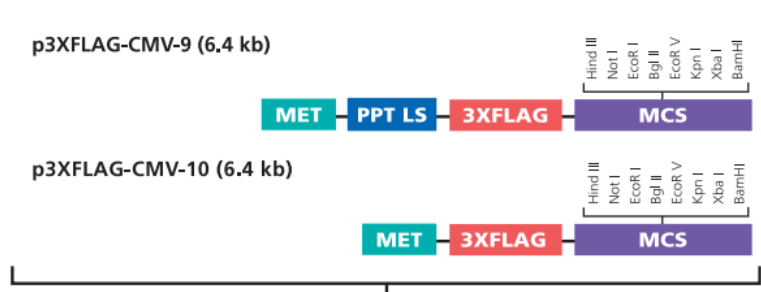
3.1.3 用HindIII与XbaI这两个酶切位点
Hind III AAGCTT
XbaI TCTAGA
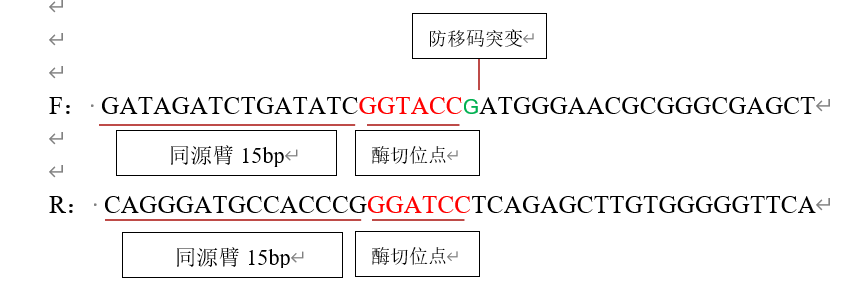
在构建表达载体的时候非常容易犯的错误在于酶切位点添加不正确导致的移码突变,因此发现测序发现100%正确,但是转染到细胞中就不能表达,这样的情况大部分是由于移码突变引起的。我们知道蛋白质是由三个碱基连在一起形成的一个读码框决定的,所以一定要保证插入序列的读码框是从ATG开始,如果一旦碱基A(或者AT)被前面的两个(一个)碱基组装在一起形成读码框,那么后面所有的氨基酸都被改变了。

这两个酶切位点保护碱基
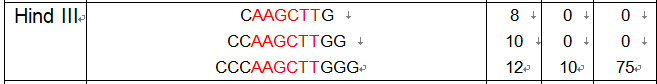
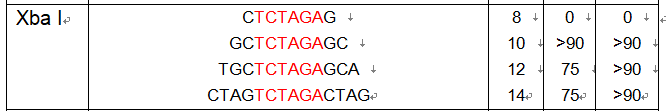
F:CCCAAGCTTATGGGAACGCGGGCGAGCT
R:GCTCTAGATCAGAGCTTGTGGGGGTTCA
4.同源重组连接(不需考虑两个酶存在于目的基因的CDS中)MCS区所有酶切位点均可以用
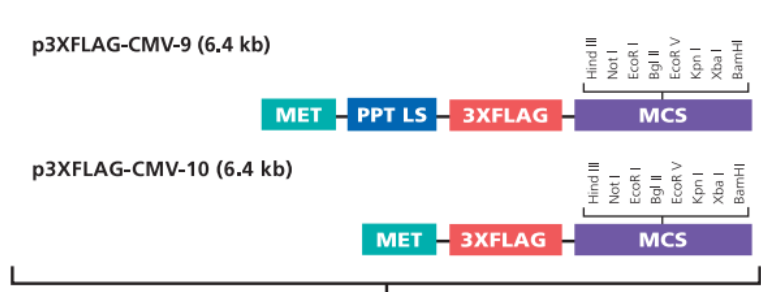
4.1 用KpnI与Bam HI这两个酶切位点
KpnI GGTACC
Bam HI GGATCC